

近日,我院入驻团队新加坡南洋理工大学邢本刚博士课题组和苏州大学高明远教授课题组合作,在实时动态的精准跟踪多种自由基信使分子并探究其病理发展过程的研究领域取得重要进展,相关成果发表在国际顶级学术期刊《自然通讯》(Nature Communications)上,我院为第一完成单位。
近年来,人们一直迫切想要全面系统地阐明严重危害人类健康的疾病机理和分子机制,以便实时追踪其发生发展过程并开发早期诊断和精准治疗的临床方案。作为细胞内关键的信使分子,生理水平的活性氧(ROS)和活性氮(RNS)自由基参与了许多重要的生理过程,如细胞通讯、信号转导、免疫代谢和炎症反应等,而过量的自由基则会导致严重的氧化损伤并介导多种疾病的形成过程。尽管这些复杂多样的自由基为全面剖析其生理病理机制提供了理想的内源标志物分子,但要在活体深层组织内实现多种自由基的同时动态跟踪并探索其与某些疾病的相关性,仍然面临艰巨挑战。
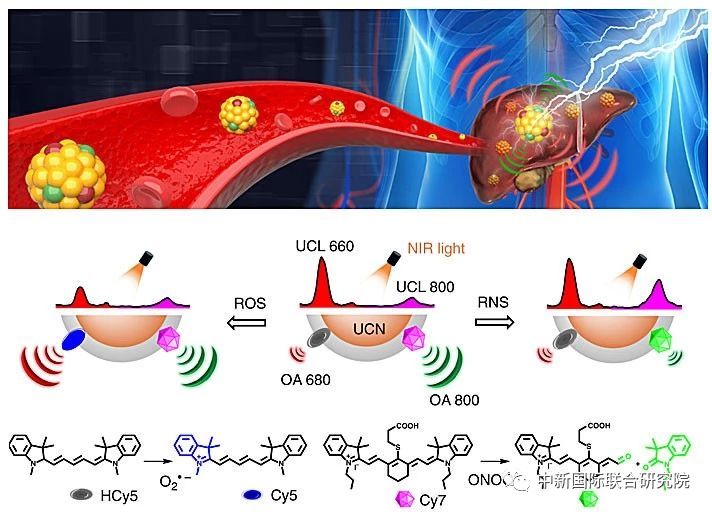
基于光声断层扫描技术(MSOT)具有的多波长吸收、深层组织穿透性以及高时空分辨率等特性,该研究团队利用稀土上转换荧光纳米粒子(UCNs),设计了一种新型的纳米探针用于多波谱光声和上转换荧光信号的实时采集和动态成像,并以此来实现多种自由基的同步跟踪并动态剖析其与药物诱发的病理损伤之间错综复杂的相关性。他们选择了两种分别对ROS(e.g., O2•-)和RNS(e.g., ONOO-)高度敏感的花青染料(HCy5和Cy7)并装载在纳米探针表面,其中HCy5会经历ROS氧化引发的结构重排并呈现增强的吸光度,而Cy7会受到RNS诱导的分子断裂而导致吸光度的降低,这种反向的变化使得利用MSOT技术实现多种自由基变化的实时比率跟踪成为可能。同时,由于染料吸收光谱与纳米载体的上转换荧光光谱(660 nm和800 nm)之间特异的荧光共振能量转移(LRET)过程,使得该探针可以利用具有深层穿透性的上转换荧光来进一步监测自由基信号的变化过程。在活体研究中,他们以小鼠药物性肝损伤为模型,对不同肝毒性药物诱发肝脏炎症过程中产生的ROS和RNS进行同时跟踪扫描,并发现在不同药物刺激下氧氮自由基之间的动态转化和平衡,从而为相关疾病的深层次实时病理剖析提供了理想的诊断平台。该研究成果有望作为新一代的非侵入式诊断技术,为人们深入探索相关疾病的生理病理机制、实现高通量的药物筛选和高效精准的临床治疗提供新颖的研究策略。
该论文作者为:Xiangzhao Ai, Zhimin Wang, Haolun Cheong, Yong Wang, Ruochong Zhang, Jun Lin, Yuanjin Zheng, Mingyuan Gao*, Bengang Xing*
原文(长按二维码或点击“阅读原文”即可直达原文页面):
Multispectral optoacoustic imaging of dynamic redox correlation and pathophysiological progression utilizing upconversion nanoprobes
Nat. Commun., 2019, 10, 1087, DOI: 10.1038/s41467-019-09001-7

文章转载自:X一MOL资讯


www.ssijri.com

朋友会在“发现-看一看”看到你“在看”的内容